Название рода
Aspergillus происходит от латинского корня
aspergillum («кропило») и таксономического суффикса
-us.
Под микроскопом аспергилл напоминает кропило, разбрызгивающее святую воду (конидии).
Видовой эпитет
oryzae — это латинское склонение слова
orȳza (родительный падеж
orȳzae), означающего «рис». Латынь заимствовала этот термин из греческого ὄρῡζα (órūza), ὄρῡζον (órūzon).
Применение
Закваска или «рисовые дрожжи», изготовленные с использованием
Aspergillus oryzae, широко используются в пищевой промышленности и биотехнологиях в Азии для осахаривания, производства ферментов и органических кислот.
Пищевая промышленность
В Японии приготовление закваски, называемой кодзи (яп. 麹), осуществляется путём засевания богатого крахмалом субстрата чистой культурой
Aspergillus, в частности
Aspergillus oryzae, для:
- приготовления саке (рисового вина) и сётю (японского зернового дистиллята);
- переработки соевых бобов для производства мисо, сёю (соевого соуса) или тамари.
Сырьём для саке служит тщательно отшлифованный рис с низким содержанием амилозы, низкой температурой желатинизации и белой сердцевиной. Эти характеристики облегчают набухание, варку и проникновение мицелия
A. oryzae. Этот рис, приготовленный на пару, смешивают с
кодзи для гидролиза в течение двух-трёх дней.
В Китае традиционные закваски
цюй представляют собой сложные культуры плесневых грибов (
Aspergillus spp., Rhizopus spp., Mucor и др.), дрожжей (
Saccharomyces cerevisiae и др.) и бактерий (
Bacillus subtilis и др.). Плесень
Aspergillus oryzae присутствует в пшеничной закваске (麦曲,
màiqū) или большой закваске (大曲,
dàqū), используемых для:
- запуска ферментации зерна и получения различных зерновых вин (хуанцзю, 黄酒), которые после дистилляции дают водку байцзю;
- запуска ферментации соевых бобов для приготовления соевого соуса (jiangyou, 酱油), мисо (weiceng, 味噌) и соуса тяньмяньцзян (甜面酱).
Производство знаменитого рисового вина Шаосин сочетает использование двух заквасок (или стартеров): кодзи (17 %), состоящего из пропаренной пшеницы, засеянной чистым
A. oryzae, и пшеничной закваски
цюй (83 %), полученной путём естественной инокуляции пшеницы[2].
Биотехнология
Aspergillus oryzae также используется в биотехнологических процессах для производства некоторых коммерческих ферментов[3][4], таких как альфа-амилаза[5], глюкоамилаза[6], протеазы[7], ксиланазы[8], глутаминазы[9], лактаза[10], кутиназа[11], липаза[10][12].
Сообщается об активности типа производства антибиотика против candida albicans[13].
Столкнувшись с проблемой выбросов парниковых газов от использования ископаемого топлива, многие исследовательские центры переориентировались на разработку биотоплива из биомассы с использованием биотехнологических процессов, вдохновлённых промышленным производством саке из рисового крахмала, разработанным Дзёкити Такамине в конце XIX века[14]. Часть биоэтанола первого поколения получают из пшеничного или кукурузного крахмала путём ферментативного гидролиза крахмала с последующей ферментацией. Зерновая мука, смешанная с водой и альфа-амилазой, проходит через варочные аппараты, где крахмал зерна разжижается. Затем добавление глюкоамилазы вызывает превращение разжиженного крахмала в сбраживаемые сахара. Добавления дрожжей достаточно для запуска спиртового брожения, производящего этанол. Производство топливного этанола из крахмалосодержащего сырья требует коммерческих амилаз, которые в настоящее время довольно дороги. Исследования[15] направлены на производство глюкоамилаз
Aspergillus oryzae путём твердофазной ферментации на дешёвых сельскохозяйственных отходах, таких как пшеничные отруби, рисовые отруби, жом сахарного тростника и т. д.
В настоящее время несколько исследовательских программ в мире направлены на использование лигноцеллюлозной части биомассы низкой стоимости (отходы сельского и лесного хозяйства), а не дорогостоящих продуктов. В природе биоразложение целлюлозы в основном осуществляется бактериями (
Ruminococcus, Clostridium и др.) и грибами (
Aspergillus,
Schizophyllum,
Penicillium,
Trichoderma…). Для промышленной реализации ферментативного гидролиза целлюлозы интерес в основном был сосредоточен на
Trichoderma reesei, который способен секретировать значительные концентрации целлюлаз (ферментов, расщепляющих целлюлозу). Чтобы устранить некоторые недостатки целлюлаз
T. reesei, можно использовать β-глюкозидазы
Aspergillus[16]. Другие методы предусматривают клонирование гена глюкоамилазы
A. oryzae или
A. niger в дрожжи[17].
Aspergillus oryzae также является основным источником нейтральных протеаз (NPI и NPII), которые проявляют высокое сродство к гидрофобным аминокислотам и, следовательно, способны устранять горечь в продуктах питания[18]. Многие отрасли пищевой промышленности используют протеазы, например, молочная промышленность[19] (для созревания сыров) или хлебопекарная для модификации пшеничного глютена путём ограниченного протеолиза. Фармацевтическая промышленность также использует протеазы
A. oryzae в качестве средств, способствующих пищеварению.
Аминопептидаза — это фермент, катализирующий отщепление аминокислоты с аминного конца белков[20]. Аминопептидаза
A. oryzae привлекла внимание, поскольку ферментативное высвобождение аминокислот и пептидов является способом усиления вкуса ферментированных продуктов. Это также гипотензивное средство.
A. oryzae способен продуцировать глутаминазу — фермент, превращающий глутамин в глутаминовую кислоту (или глутамат), один из основных компонентов вкуса соевого соуса.
Поскольку некоторые люди плохо переносят молочный сахар (или лактозу), были разработаны программы производства молока с низким содержанием лактозы. Фермент, гидролизующий лактозу (или лактаза), может быть получен из
A. oryzae, который считается безопасной плесенью.
Первым промышленным производством фермента[11] с помощью
A. oryzae стала липаза для стиральных порошков в 1988 году. В сыроделии липаза, гидролизуя жиры, способствует усилению вкуса сливок и сыров.
| Ферменты | Класс | Промышленное применение | Примечание |
|---|
Некоторые примеры ферментов, продуцируемых A. oryzae путём ферментации
(по данным BRENDA[4], Pariza et al[3], Belmessikh[18]) | | | |
| α-амилазы | Карбогидраза | Хлебопечение, глюкозные сиропы | [5] |
| Глюкоамилазы | Карбогидраза | Хлебопечение, саке, сёю, биоэтанол | [6] |
| Протеазы | Протеаза | Соевый соус, сыроделие, хлебопечение, кожевенное дело | |
| Аминопептидаза | Протеаза | Вкусовая добавка | [20] |
| Ксиланазы | Гидролаза | Биоотбеливание, хлебопечение | [8] |
| Глутаминазы | | Соевый соус, лечение лейкемии | [9] |
| Лактазы | Карбогидраза | Гидролиз кислой сыворотки | [10] |
| Кутиназы | Гидролаза | Переработка биоразлагаемых пластиков | |
| Липазы | Липаза | Сыроделие, стиральные порошки | [10] |
История
В конце XIX века немецкий профессор Герман Альбург, приглашённый преподавать в Медицинскую школу Токио, проанализировал закваску кодзи, используемую для производства саке. Он идентифицировал в кодзи плесень, которую назвал
Eurotium oryzae Ahlburg (в 1876 году) и которая затем была переименована в 1883 году немецким микробиологом Фердинандом Юлиусом Коном в
Aspergillus oryzae (Ahlburg) Cohn. Полное морфологическое описание было дано только в 1895 году Вемером.
Морфология и физиология
Как и все
Aspergillus,
A. oryzae образован сетью гиалиновых нитей (мицелием) тонкого и регулярного диаметра, септированных (разделённых перегородками) и разветвлённых[21]. На этих нитях возникают вертикальные нити, которые не имеют перегородок и заканчиваются везикулой, на которой расположены конидиогенные клетки (образующие споры или конидии). Эти споры, образующиеся путём митотического деления, обеспечивают бесполое размножение гриба.
A. oryzae быстро развивается на классических средах (солодовый агар и агар Сабуро) при 22—25 °C. Он образует пушистые или порошкообразные колонии, сначала белого цвета, затем жёлтого и, наконец, желтовато-зелёного.
Секвенирование генома
Aspergillus oryzae, некоторое время державшееся в секрете, было окончательно опубликовано в 2005 году группой японских биологов из Цукубы[22]. Он содержит 12 074 гена, что на 7—9 миллионов оснований ДНК больше, чем у
A. fumigatus и
A. nidulans. Эти дополнительные гены предположительно участвуют в синтезе и транспорте многих вторичных метаболитов, не участвующих напрямую в росте и нормальном размножении[23]. Сравнение нескольких геномов
Aspergillus показало, что
A. oryzae (и
A. fumigatus) содержат гены полового типа.
Токсикология
A. oryzae продуцирует ряд вторичных метаболитов, известных своей токсичностью для человека[24].
Циклопиазоновая кислота может быть выделена из культуры
A. oryzae на твёрдой или жидкой среде. Эта кислота нарушает функцию саркоплазматического ретикулума. Допустимая суточная доза для человека составляет 700 мкг/день.
Койевая кислота продуцируется многими штаммами
Aspergillus и
Penicillium. Она не опасна в дозах, присутствующих в продуктах питания. Аспергилломаразмин был выделен из
A. oryzae как фитотоксин. Было показано, что он оказывает ингибирующее действие на ангиотензинпревращающий фермент (АПФ). 3-нитропропионовая кислота, продуцируемая
A. oryzae, является нейротоксином, приводящим к дисфункции митохондрий.
Производство афлатоксина грибом
A. oryzae было предметом споров. Афлатоксины являются опасными природными канцерогенами, которые могут загрязнять семена арахиса, кукурузы, пшеницы и т. д. В настоящее время установлено, что
A. oryzae не продуцирует афлатоксины, а ошибочные идентификации были связаны с неправильным определением
A. oryzae и путаницей со штаммами, очень близкими в таксономическом отношении к группе
A. flavus.
В то время как
A. flavus и
A. parasiticus являются основными продуцентами афлатоксинов,
A. oryzae, не продуцирующий афлатоксин, считается безопасным или GRAS (Generally recognized as safe) по классификации FDA[11].
| Метаболит | ЛД50 (мг/кг) | Путь |
|---|
Вторичные метаболиты, продуцируемые A. oryzae, и ЛД50
по данным C. Blumenthal[24], 2003; ИП — внутрибрюшинно, ВВ — внутривенно, О — перорально | | |
| Циклопиазоновая кислота | 2 (крыса)
64 (мышь) | ИП
О |
| Койевая кислота | 250 (мышь) | ИП |
| Аспергилломаразмин | 160 (мышь) | ВВ |
| 3-нитропропионовая кислота | 67 (крыса) | ИП |
| Виолацетин | 45 (мышь) | ИП |
Механизм действия
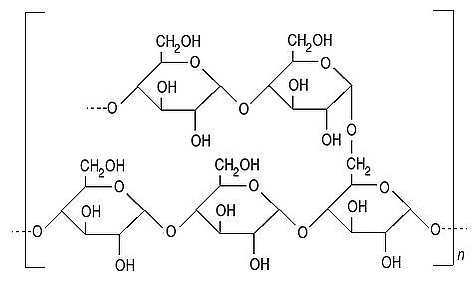

Структура амилопектина со связями α(1→4) в основной цепи, соединённой связями α(1→6) с разветвлениями
Aspergillus инициирует расщепление крахмала, содержащегося в зерне, производя сахара, которые, в свою очередь, обеспечат ферментацию с помощью дрожжей или бактерий. Это осахаривание обусловлено секрецией особой амилазы, α-амилазы или такадиастазы, которая гидролизует крахмал варёного зерна за два-три дня. Затем начинается собственно спиртовое брожение под влиянием дрожжей, попадающих из воздуха.
Крахмал образован остатками глюкозы (D-ангидроглюкопиранозы), соединёнными между собой либо связями α(1→4), либо связями α(1→6), которые являются причиной разветвлений в структуре молекулы. Он состоит из двух полисахаридов: амилозы и амилопектина. Амилоза представляет собой полимер остатков глюкозы, соединённых гликозидными связями α(1→4), тогда как амилопектин — это разветвлённая молекула с длинными ветвями каждые 24—30 единиц глюкозы, связанными посредством связей α(1→6).
Учёные идентифицировали 71 белок, секретируемый штаммом SU16
A. oryzae, используемым для производства вина Шаосин[2]. Многие из них являются ферментами, участвующими в гидролитическом расщеплении крахмала (α-амилазы, глюкоамилазы B и продукты их протеолиза), белков, клеточных стенок и т. д. Среди протеолитических ферментов наиболее распространены оризин, пепсин, нейтральная протеаза II и аланил-дипептидилпептидаза. Профиль секретируемых белков варьируется в зависимости от среды культивирования.
α-амилаза — это гликозидаза, которая расщепляет α-1,4-глюкозидные связи субстрата случайным образом в середине цепей. Этот гидролиз высвобождает в основном мальтозу, изомальтозу, мономеры глюкозы и остаточные декстрины. Декстрины не сбраживаются. Тогда как мальтоза и изомальтоза (состоящие из двух единиц глюкозы) и сама глюкоза являются сбраживаемыми. α-амилаза называется «щелочным протеолитическим» ферментом, так как она действует в щелочной среде как природный фермент, способствуя пищеварению. Существует мнение, что архаичное производство саке зависело от слюны (слюнной амилазы) молодых девственниц, которым поручалось пережёвывать рис, чтобы пропитать его слюной.
Глюкоамилаза (или γ-амилаза) высвобождает единицы глюкозы одну за другой, начиная с невосстанавливающего конца атакуемого полимера. Она полностью гидролизует амилопектин и амилозу до D-глюкозы. Она способна гидролизовать как связи α(1→6), так и связи α(1→4) или α(1→3). Глюкоамилазы продуцируются
A. oryzae при ферментации на твёрдом субстрате, таком как поверхность пшеничных отрубей, рисовых отрубей или муки из семян хлопка и т. д. Они в основном используются в промышленном производстве глюкозного сиропа, кукурузного сиропа с высоким содержанием фруктозы и спирта[17].
















